- Функции молочной железы
- Железистая ткань
- Выводящие протоки
- Внешний вид вымени
- Образование молока
- Молокоотдача
- Проведение исследований
- Рецепт 4 Среда Гисса с манитом
- Диагностика и уход за выменем
- Уход за выменем
- Среда для анаэробной ферментации сахаров
- Определение лизоцимов молока по в.И.Мутовину
- Лечение животных, больных маститом.
- Физиотерапия
Функции молочной железы
Вымя у КРС претерпело сильные изменения в процессе селекционного отбора. При выведении молочных пород скота отбирались животные с лучшими показателями по лактации. В результате были получены коровы с большой, объемной молочной железой, позволяющей производить и накапливать до 40 литров и более.
Железистая ткань
Основу вымени составляют железы – выстланные секреторными клетками альвеолы. Они находятся в оплетении звездчатыми клетками, отвечающими за выделение молока – сокращаясь, они инициируют процесс молокоотдачи.
https://www.youtube.com/watch{q}v=OtRkcvf8xs0
Молоко продуцируется альвеолами из крови, поэтому вымя богато кровеносными сосудами. В период активной лактации за одну минуту через молочную железу проходит более 4 литров крови. Она поступает из промежностных артерий – это общая система с кровоснабжением репродуктивных органов. Это позволяет контролировать молокообразование половыми гормонами, но и становится причиной вторичных инфекций вымени при патологиях матки.
Выводящие протоки
Продуцируемое альвеолами молоко выводится наружу по сети каналов. После сокращения звездчатых клеток, перемещение идет по протокам (мелким и средним).
Средние протоки и альвеолы образуют дольки вымени – структурные единицы молочной железы.
Некрупные протоки объединяются в молочные ходы, по которым секрет поступает в цистерну. В ней молоко накапливается до доения. Расположены цистерны в основании сосков – конических ответвлений молочной железы с протоком в центре.
Соски трехслойны – снаружи покрываются лишенной волос кожей, изнутри выстланы слизистой, а между ними находится соединительная ткань с разносторонними пучками мышечных волокон. В покое соски закрыты – в верхушке просвет сжат сфинктером, а по всей длине образованы складки.
Внешний вид вымени
Совокупность железистой ткани, выводящих путей, кровеносных сосудов и нервных волокон, покрывающих их мышц и кожи, называется выменем. У коров оно состоит из четырех долей, но бывают и добавочные. Чаще всего они не развиты и внешне проявляются небольшими сосками. В норме у коровы 4 соска, которые являются продолжением развитой и функционирующей четверти.
Снаружи молочная железа покрывается гладкой и эластичной кожей. Волосы в данной области нежные и короткие, формирующие за счет особенности роста на задней поверхности молочное зеркало – экстерьерный показатель высокой продуктивности.

По форме выделяется 5 типов молочной железы:
- чашеобразный – самый распространенный, характеризуется правильностью формы, высокой молочностью;
- ваннообразный – вытянутый вдоль брюшной стенки тип вымени, характерен для пород с высокой продуктивностью – голштинская (на фото), черно-пестрая;
- округлый – отличается меньшей площадью прикрепления в сравнении с объемом. Часто отвисает, создавая препятствия перемещению, легче загрязняется и чаще подвержено маститу;
- козий – вытянутое вымя в форме треугольника. Доли железы развиты слабо, крупный рогатый скот показывает низкую продуктивность, плохо раздаивается;
- примитивный – недоразвитое, характерное для непородных животных и коров мясной продуктивности.
Работа вымени тесно связана с процессами воспроизводства. У молочной железы выделяются два основных процесса – образование и отдача молока, а в первые дни лактации – молозива. Эти процессы взаимосвязаны – своевременное сдаивание молока провоцирует его образование.
Функциональность вымени подчиняется половым гормонам – прогестерон, эстроген, окситоцин.
Образование молока
Начало лактации совпадает с родами. Процесс молокообразования регулируется двумя факторами. Во-первых, это гормональное и нейротропное воздействие:
- гипофиз;
- яичники;
- надпочечники;
- щитовидная железа.
Во-вторых, внешние раздражители. Это и стимуляция сосков доильными стаканами или теленком, и кормление, шум, стрессовые факторы. Многообразие факторов образования молока объясняет периодические колебания удоя.
Таким образом, для стабильного повышения надоя необходимо дойку проводить в одно и то же время. Животным с высокой продуктивностью следует организовывать трехкратную дойку. В кормлении следует избегать резких перемен и использование недоброкачественной пищи.
Кроме образования молока, вымя вырабатывает еще одно важное вещество – молозиво. Оно продуцируется в первое время после родов и обеспечивает новорожденного теленка большим количеством жира, витаминами, сахаром. Но главное отличие молозива от молока – большое содержание белков (до 20% в сравнении с обычным в 3%). Это обеспечивает теленка нужным количеством антител, формируя у него колостральный иммунитет.
Молокоотдача
Перемещение секретов вымени от альвеол через мелкие протоки в соски называется отдачей молока. Процесс выделения начинается после раздражения кожи сосков и вымени обеспечивающего приток крови к органу.
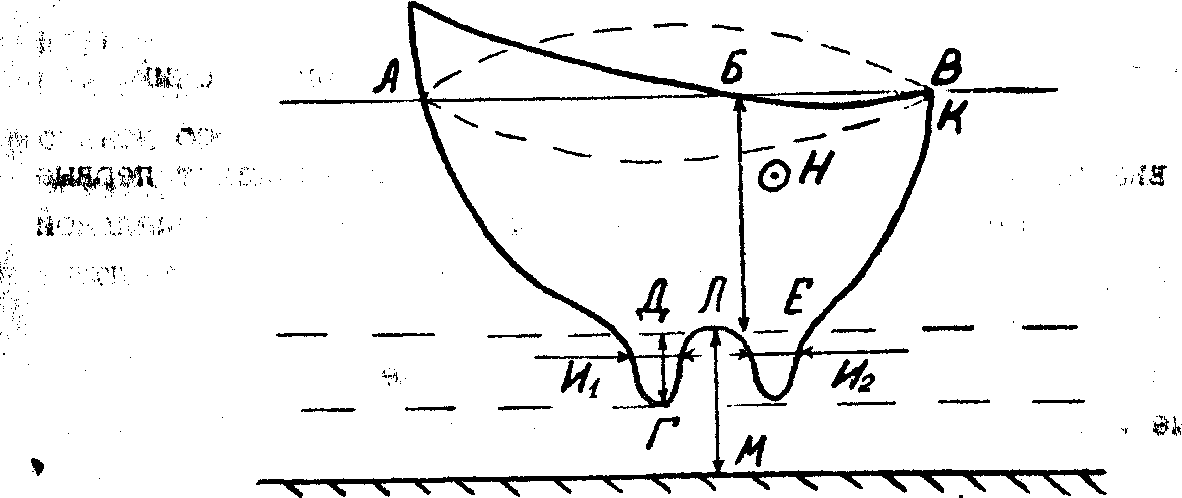
Это состояние эрекции молочной железы стимулирует отделение секрета, раскрытие сфинктера и последовательное сокращение гладкой мускулатуры. Последующее доение или сосание усиливают раздражение, что повышает образование окситоцина, ускоряющего выделение молока.
Проведение исследований
Бактериологическое
исследование молока (секрета) проводят
сразу после доставки его в лабораторию.
Оставшееся молоко хранят при температуре
не выше 6°С.
Посев молока
(секрета) проводят на мясо-пептонный
агар с цитратной кровью крупного рогатого
скота или дефибринированной кровью
барана (рецепт 1)и
дифференциально-диагностические или
элективные среды.
Для идентификации
выросших культур микроорганизмов
учитывают характер роста колоний и вид
гемолиза на кровяном МПА, проводят
микроскопию мазков, сделанных из
одинаковых по морфологическим свойствам
колоний и окрашенных по Грамму, изучают
культурально-биохимические свойства.
а) Выделение
золотистого стафилококка
Рост на кровяном
МПА. Колонии средние и крупные, выпуклые
с гладкой или шероховатой поверхностью,
ровными краями, золотистого цвета.
Образуют зону
гемолиза.
α-гемолиз
-зона прозрачная вокруг колонии;
β-гемолиз -зона непрозрачная
(матовая.),лучше проявляется
при выдержке посевов в холодильнике
при температуре 5-8°С в течение
24ч; α и β гемолиз смешанный.
При микроскопии
имеют шарообразную форму и располагаются
в виде гроздевидных скоплений, тетрами
или одиночно. По Грамму красятся
положительно.
ДНК-азная активность.
Выделение золотистого стафилококка
ускоренным методом и определение
ДНК-азной активности проводят с
использованием элективной,
дифференциально-диагностической среды
ДНК-новокаинового агара (рецепт
2).
Элективные свойства
среды обусловлены ингибирующим действием
на постороннюю микрофлору новокаина,
дифференцирующие -наличием
ДНК, позволяющей идентифицировать
золотистый стафилококк по его
дезоксирибонуклеазной активности.
Готовят разведение
исследуемых проб молока, (секрета) на
стерильном физиологическом растворе
1:10и 1:100.В чашку Петри
с ДНК-новокаиновым агаром вносят
0,1мл молока (секрета) в разведении
1:100и равномерно распределяют
стерильным стеклянным шпателем по
всей поверхности питательной среды.
Засеянные чашки помещают в термостат
крышками вниз и инкубируют при 37-38°С в
течение22-24ч. Для выделения
ДНК-азной активности золотистого
стафилококка поверхность среды в
чашках с выросшими культурами заливают5-7мл 1н раствора соляной
кислоты. Чашки с кислотой выдерживают2-3мин, затем кислоту
сливают и учитывают результаты,
просматривая чашки в проходящем
свете.
При выделении
культуры стафилококка на кровяном агаре
и наличии изолированной чистой
культуры ДНК-азная активность может
быть определена путем посева на ДНК-агар
(рецепт 3).
На ДНК-новокаиновом
агаре золотистый, стафилококк растет
в виде крупных круглых колоний с ровными
краями, окруженных зоной просветления
с четкими границами.
Для определения
количества золотистого стафилококка
в 1мл исследуемого молока
(секрета) подсчитывают колонии с зоной
просветления по всей поверхности
среды и полученное число колоний
умножают на 10(брали
0,1мл материала) и на 100(степень разведения).
Каталазная
активность.
На предметное стекло наносят каплю 10%
перекиси водорода и в ней растирают
внесенную бактериологической петлей
чистую культуру микроорганизмов.
При положительной
реакции на каталазу происходит интенсивное
газообразование которое проявляется
вспениванием капли перекиси водорода.
Фермент каталазу содержат стафилококки
и микрококки.
5и разливают в аглютинационные
пробирки по 0,5мл. Бульонную
культуру стафилококка по 0,1мл (2капли) вносят в
пробирки с разведенной кроличьей
плазмой. Для контроля в одну пробирку
с плазмой не вносят культуру, а в
другую засевают заведомо плазмо-аглютинирующий
стафилококк. Пробирки помещают в
термостат при температуре 37°С и через
каждый час в течение 3ч, 18и 24ч учитывают результаты.
При положительной
реакции РПК образуется сгусток, который
не выпадает из пробирки при наклоне или
плавает в плазме.
Золотистый
стафилококк является плазмокоагулируюшим.
Ферментация
манита в анаэробных условиях.Суточную
бульонную культуру стафилококка в
количестве 0,2мл(3-4капли) высевают в пробирку с
0,15% полужидким агаром, содержащим
0,15%манита и индикатор Андраде, под
вазелиновым маслом (рецепт
4).Посевы инкубируют в термостате
при температуре 37°С. Результаты учитывают
через каждые 24 ч, а окончательный
результат -через
5сут.
Появление розового
окрашивания (изменение цвета индикатора)
указывает на ферментацию манита в
анаэробных условиях, что является
дифференцирующим признаком для
золотистого стафилококка.
б) Выделение
стрептококков
Рост на 5% кровяном
МПА.Колонии мелкие, росинчатые,
образуют зону гемолиза α и β, смешанную
или она отсутствует.
При микроскопии
имеют шарообразную, бобовидную форму
и располагаются в виде коротких или
длинных цепочек.
Рост на среде
Карташовой (рецепт 5).В пробирку со средой вносят
1мл исследуемого молока или пересевают
выросшие на кровяном агаре росинчатые
колонии и инкубируют в термостате при
температуре 37°С в течение
18-24ч.
Из пробирок с
измененным цветом среды делаютмазки,окрашивают по Грамму и проводят
микроскопию на предмет обнаружения
стрептококков.
Каталазная
активность.Проводится аналогично
как для стафилококков.
Стрептококки не
содержат фермент каталазу, поэтому с
перекисью водорода дают
каталазоотрицательную реакцию.
Устойчивость к
желчи.Предварительно культуру
стрептококков выращивают в мясо-пептонном
бульоне (МПБ) с I%глюкозы
(рецепт6),а затем вносят
1мл культуры в пробирки с
5мл МПБ, содержащего
40% желчи (рецепт 7)и
ставят в термостат при температуре 37°С
на 24ч.
Полное просветление
бульона указывает на лизис культуры,
помутнение -на рост.
Рост в МПБ с рН
9,б. 1млбульонной культуры
стрептококков, выращенных на МПБ с
глюкозой (рецепт 6),вносят
в пробирку с 5мл МПБ и рН
9,6,инкубируют в термостате при
температуре 37°С в течение
24ч.
Обесцвечивание
среды указывает на наличие роста
стрептококков, восстанавливающих
своими окислительно-восстановительными
ферментами метиленовый синий.
Этим свойствам
обладают стрептококки серологических
групп Dи N.(по Ленсфильд).
КАМП-тест.Основан на том, что стрептококки групп
В при выращивании на кровяном агаре,
содержащем стафилококковый β-токсин,
образуют дополнительную, ясно выраженную
зону гемолиза эритроцитов барана,
крупного рогатого скота.
Суточную бульонную
культуру β-гемолитического стафилококка
высевают на 5%кровяной
агар сплошной линией по диаметру чашки
Петри. Перпендикулярно к линии посева
стафилококка, не доходя 5-6
мм,высевают ровным штрихом
испытуемую культуру стрептококков. На
одной чашке можно проверить
8-10культур.
КАМП-тест считают
положительным, если четко выражена зона
гемолиза испытуемого стрептококка в
виде усеченного треугольника или
полукруга в зоне β-гемолитического
стафилококка. Наиболее ярко эта зона
проявляется после выдержки чашек в
холодильнике в течение
18-84.
в) Выделение
бактерий группы кишечной палочки (БГКП).
Образцы молока
или колоний с кровяного агара,
морфологические свойства которых
напоминают БРКП, высевают на среду КОДа
(рецепт 9)и помешают в
термостат при температуре 35°С на
24ч.
Изменение цвета
среды из фиолетового в зеленый
свидетельствует о наличии ВГКП.
Идентификацию
эшерихий, бактерий рода энтеробактер
от сальмонелл и протея проводят на среде
Олькеницкого (рецепт 10).Со среды КОДазеленого
цвета посев на среду Олькеницкого в
пробирках проводят бактериологической
петлей на поверхность скоса среды и
внутрь столбика. Посевы инкубируют в
термостате при температуре 37°С в течение
24ч.
Изменение цвета
(глюкоза , лактоза ) скоса и столбика
среды из красного в желтый при отсутствии
почернения внутри свидетельствует
о росте бактерий группы эшерихий.
Изменение скоса
среды и столбика в малиновый цвет
(мочевина ) и почернение внутри столбика
(сероводород ) указывает на рост протея.
https://www.youtube.com/watch{q}v=6PiHd4n8fWc
Изменение скоса
в красный, столбика в желтый и почернение
внутри столбика указывает на рост
сальмонелл.
г) Выделение
синегнойной палочки.
Бактерии этой
группы при росте на питательных средах
вырабатывают сине-зеленый пигмент
-пиоцианин за счет которого
происходит окрашивание этих сред.
Образцы молока
или колоний с кровяного агара, при
микроскопии которых обнаружены
грамотрицательные палочки, высевают
на МПА и МПБ, культивируют в термостате
при температуре 37°С в течение 24-48ч, дополнительно до 72 ч.
Появление
сине-зеленого окрашивания МПБ и МПА,
роста гладких плоских колоний с ровными
или изрезанными краями указывает на
рост синегнойной палочки, вырабатывающей
пигмент пиоционин.
Из МПБ и МПА делаютмазки,окрашивают по Грамму и
просматривают под микроскопом.
При обнаружении
в мазках грамотрицательных палочек и
изменении цвета сред в сине-зеленый
ставят реакцию для обнаружения пиоционина.
Определение
пиоционина. В пробирку с МПБ добавляют
1млхлороформа, пробирку
встряхивают.
При положительной
реакции хлороформ приобретает зеленый
цвет и опускается на дно пробирки.
https://www.youtube.com/watch{q}v=vrKaRU8qrjs
У пигментообразующих
сапрофитных бактерии в хлороформе
пигмент не растворяется.
д) Выделение
грибов рода Саndida
Пробы молока в
количестве по 0,1-0,3мл
высевают на 2чашки Петри
с элективной дифференциально-диагностической
средой (рецепт11),равномерно
распределяя материал по поверхности
стерильным шпателем.
Засеянные чашки помещают в термостат
вверх дном при температуре 37°С на
18-20ч.
Контролем служит
посев культуры этого гриба на ту же
самую элективную дифференциально-диагностическую
среду.
После инкубации
чашки Петри просматривают, из подозрительных
колоний делают мазки, окрашивают их по
Грамму или другими методами, а также
делают посев на ту же самую среду для
выделения чистой культуры и выявления
псевдомицелия. Засеянные пробирки
выдерживают в термостате при
температуре 37°С в течение 24ч, затем выдерживают при комнатной
температуре 2суток.
Рецепт 4 Среда Гисса с манитом
ДНК-агар
К 150мл расплавленного 2%МПА
(рН 8,6)добавляют
150мг ДНК-натриевой соли, растворенной
в 10мл дистиллированной
воды (подщелоченной 2каплями 10%едкого натра).
Среду прогревают 30 мин в
кипящей водяной бане, затем охлаждают
до 50-60°С и добавляют 1,2мл 10% стерильного раствора хлористого
кальция и 13-14мл(8-9%)сыворотки крови крупного рогатого скота
или 8мл (5%)
дрожжевого экстракта.
0,5г кислого фуксина растворяют в
100мл стерильной дистиллированной
воды, добавляют 16,4мл 1н
едкого натра, стерилизуют при 100°С
5мин, хранят в темном месте с притертой
пробкой.
Рецепт
5
Диагностика и уход за выменем
Исследование молочной железы начинается со сбора анамнестических сведений. При этом следует установить:
- особенности беременности – ее течение, процесс родов, подготовка к лактации;
- общее состояние;
- особое внимание уделяется половой системе;
- перенесенные ранее патологии вымени;
- статистика удоя, жирности и содержания белка;
- качество молока;
- время наступления болезни.
Обследование коровы начинается с общей диагностики, затем переходят к пальпации и осмотру вымени. Осмотр молочной железы производят сбоку и сзади, обращая внимание на молочное зеркало и общее состояние волос и кожи, наличие повреждений, эрозий и язв.
Пальпацией выявляют:
- местную температуру на различных участках тыльной стороной ладони;
- болезненность отдельных участков;
- консистенцию;
- качество кожи.
Особое внимание уделяется лимфатическим узлам. Их ощупывают на задней поверхности рядом с сагиттальной линией. В норме они должны быть подвижными и не превышать 3-4 см в диаметре. В патологическом состоянии их консистенция становится плотной, они болезненны и неподвижны.
Обследование завершают исследованием сосков. Для этого его захватывают у основания и вытягивают, смещая пальцы к верхушке. Сосок раскатывают для выявления морфологических нарушений, наличие молочных камней и изменений в цистерне. Исследование тонуса молочного канала и сфинктера делают путем пробного выдаивания.
Уход за выменем
Перед дойкой необходимо вымыть молочную железу. Это необходимо для предотвращения обсеменения получаемого молока микроорганизмами и грязью. Также, осуществляя гигиену вымени, производится его массаж, что активизирует молокоотдачу. Для ухода используют средства на основе поверхностно активных веществ и йода.
Обработка после дойки направлена на предупреждение проникновение микрофлоры в молочную железу, восстановление ее функциональности после механического воздействия. Для этого используют крем для вымени коров, проявляющий такие свойства:
- устранение сухости кожи;
- смягчение и восстановление эластичности;
- избавление от зуда при укусах паразитами;
- снятие болезненности и воспалительного процесса;
- активация восстановительных процессов – заживление ран и трещин;
- снижение риска развития маститов и отеков вымени.
Также крема и другие средства гигиены молочной железы образуют тонкую пленку на ее поверхности, что препятствует проникновению микробов. Но это способствует развитию анаэробной микрофлоры, поэтому следует ограничить их применение при травмах.
Среда для анаэробной ферментации сахаров
25г
дрожжей растворить в 100мл дистиллированной воды, прокипятить
45мин, затем после охлаждения
центрифугировать при 3000
об/мин в течение 45мин.Слить в колбу и довести до
кипения. Разлить в стерильные пробирки
и поставить в термостат при 37°С на24ч.
На 1л дистиллированной воды внести
10г трипсина Дифко, 1 мл
экстракта дрожжей, 10г
манита (глюкозы), 2г
агар-агара и0,04г
бромкрезолпурина, довести до кипения,
затем стерилизовать в автоклаве при
0,5атм. в течение 20мин. Разлить в пробирки до высоты
10-12см.
Рецепт
13
Кровяной агар с
эскулином
В 1мл МПБ вносят
5г хлорида натрия, 1г эскулина (получают из конского каштана),
20г агар-агара.
В стерилизованную
при 121°С среду в течение 15мин с рН 7,4, охлажденную
до 45-48°С, добавляют 50мл
дефибринированной крови барана, хорошо
перемешивают и разливают в чашки Петри.
Чашки со средой выдерживают в термостате
при 37°С в течение 24ч с
целью просушивания и проверки стерильности.
Чашки хранят в холодильнике при
температуре 4-б°С и используют в течение
15дней со дня приготовления.
Рецепт
14
Водный раствор
пептона
3г
пептона помещают в колбу и доливают до
100мл водопроводной водой,
стерилизуют при 121°С в течение
10мин и хранят в холодильнике при
температуре б-8°С в течение
30суток.
Определение лизоцимов молока по в.И.Мутовину
В основе выявления
лизоцимов положен метод диффузии в агар
и образования зоны задержки роста (ЗЗР)
тест-культуры микроба. На агаровую
пластинку в чашке Петри наносят по
0.2мл суточной бульонной
тест-культуры и равномерно распределяют
по всей поверхности. Выдерживают
20-30мин при комнатной температуре
для пропитывания агара, а затем с
помощью пробойника диаметром
0,8-1см делают 4луночки, в которые вносят по
0,01мл (2капли)
исследуемого молока. Чашки выдерживают
при комнатной температуре (18-20°С)30-40мин, а затем 16-18ч в
термостате при температуре 36-38°С, после
чего измеряют ЗЗР
а) «Лизоцим
молока» – ЛМ
В качестве
тест-культуры используют золотистый
стафилококк штамм ВМ- 57,выделенный из молока здоровой коровы.
Максимальный
уровень ЛМ (25мм и более)
у здоровых коров на2-6месяцах лактации, у больных
-понижен (менее 18мм)
или отсутствует (0).Термостабилен, разрушается при температуре
70°С, в сыром молоке сохраняется до
10дней при температуре 4-6°С.
б) «Лизоцим
вымени» – ЛВ
В качестве
тест-культуры используют слезный
микрококк Флеминга.
Не коррелирует с
ЛМ, повышается уровень в молоке в конце
лактации и у больных маститом коров. В
сыром молоке сохраняется до
10дней при температуре 4-б°С.
в) «Лизоцим
колостральный» -ЛК
В качестве
тест-культуры используют белый стрептококк
штамм.
Максимальные
концентрации ЛК в молозиве, через
10дней после отела его уровень ниже
уровня ЛМ.
г) «Лизоцим
термостабильный» -ЛТ
В качестве
тест-культуры используют золотистый
стафилококк штамм ВМ-57.
Выявляется в молоке
стародойных коров после прогревания
при температуре 70°С в течение
30мин и сохраняется до
1,5-2,0мес., в сыром
молоке сохраняется 5-7дней
д) «Лизоцим
инверсионный» -ЛИ
В качестве
тест-культуры используют розовый
стафилококк штамм 56.
Отсутствует в
молоке здоровых коров, обнаруживается
в секрете пораженных маститом долей
вымени.
е) «Лизоцим
основной»- ЛО
В качестве
тест-культуры используют ацидофильную
палочку штамм 17т. Определяют
методом серийных разведении. В разведения
молока (молозива) вносят в объеме 10%
суточную бульонную тест-культуру,
выдерживают в термостате при температуре
37°С в течение суток, после чего учитывают
рост.
В молозиве ЛО
действует бактерицидно в разведении
1:10 000, на 10-й день после отела в молоке
его антибактериальное действие
проявляется в разведении
1:2-1:4,а у больных маститом коров ЛО
несколько повышается.
Лечение животных, больных маститом.
Лечение коров
при клинически выраженных маститах.
Терапию осущсстнляют, учитывая форму,
течение воспаления вымени,
причинывозникновения, общее состояние
животного. Наиболее эффективно
лечение маститов в первые дни заболевания.
Необходимо соблюдать осторожность в
дозировании лекарственных препаратов
и применении некоторых процедур.
Во время лечения
одновременно применяют две-три процедуры
с учетом их сложности и действия на
организм. Постоянное наблюдение за
больными животными позволяет определить
эффективность терапии и в случае
необходимости изменить способ
лечения.
При острых маститах
коров изолируют, переводят на ручное
доение, пораженные четверти выдаивают
последними в отдельную посуду, секрет
уничтожают, а посуду обеззараживают.
С целью уменьшения секреции молока
коров переводят на диету
— уменьшают
дачу концентрированных и сочных кормов,
заменяя их доброкачественным сеном,
ограничивают водопой.
Моцион коровам
предоставляют с учетом формы мастита
и течении заболевания.
Для лечения маститов
у коров предложено большое количество
методов, из которых наиболее эффективна
патогенетическая терапия. Ветеринарный
специалист должен научно обоснованно
выбирать метод лечения, учитывая
возможность его выполнения в данных
условиях.
Физиотерапия
Физические методы
лечения предусматривают применение
холода в первые сутки воспаления вымени
для снижения болевой реакции, уменьшения
выпота из кровеносных сосудов жидкой
части крови в ткани вымени. Пораженную
четверть обливают холодной водой,
обмазывают жидкой глиной с уксусом
(2—3 столовых
ложки на
1 л воды);
если глина высыхает, ее поливают
холодной водой. Холод применяют не
более
3—4 ч.
Осторожное
сдаивание
пораженной четверти вымени, т. е. через
каждые
2—3 ч,
показано при всех формах мастита. Оно
обеспечивает опорожнение цистерны,
удаление с секретом токсических
веществ и возбудителей заболевания,
уменьшает внутривыменное давление,
снижает болевую реакцию, что положительно
влияет на процесс выздоровления.
Массаж вымени
применяют при серозном мастите снизу
вверх, чтобы улучшить отток крови и
лимфы, при катаральном
— сверху
вниз для лучшего перемещения сгустков
и экссудата из молочных ходов в
цистерну и выведения их из
вымени при
доении. Массаж способствует ускорению
рассасывания воспалительной
инфильтрации, активизирует
нервно-рефлекторные процессы в
молочной железе, улучшает обмен веществ,
лимфо- и кровообращение, увеличивает
приток питательных веществ к тканям.
Если в цистерне
больной четверти скопилось много
труд-ноудаляемых сгустков и хлопьев,
препятствующих сдаиванию, то для их
разжижения вводят в вымя
40—50 мл
теплого 2—3%-ного
раствора соды или 1—2%-ного соле-содового
раствора. Вымя слегка встряхивают и
через
20—30 мин
сдаивают. Не рекомендуется частое
проведение катетеризаций, так как
длительное раздражение воспаленной
слизистой оболочки может вести к
сужению сокового канала и цистерны.
Тепло
назначают на
3—5-й день
при ослаблении воспалительной реакции
в стадии разрешения воспалительного
процесса. Для этого применяют
согревающие компрессы, парафино- и
озокеритотерапию, тиосульфатную грелку,
а также облучение лампами соллюкс и
инфраруж. Под воздействием тепла
усиливаются трофические процессы и
ускоряется рассасывание воспалительного
инфильтрата.
Для согревающих компрессов
лучше использовать винный или камфорный
спирт, способ наложения компресса
обычный. При парафинотерапии на чистую,
сухую кожу вымени с выстриженным
волосяным покровом наносят широкой
кисточкой расплавленный парафин
температурой
60 °С. На
образовавшийся слой наносят еще несколько
слоев парафина, подогретого до 900
С.
Для
удержания тепла поверх парафина
накладывают клеенку, затем слой ваты и
марли. Процедуру повторяют ежедневно.
При озокеритотерапии озокерит, нагретый
до
100— 110°С,
разливают в кюветки, на дне которых
находится клеенка, слоем
1,5—2,5 см.
Размер первой кюветки
46х46 см,
второй—66х66
см.
Озокерит из второй кюветки температурой
65—70
°С прикладывают к чистой, сухой коже
пораженной четверти вымени. Чтобы
дольше сохранить тепло, поверх пленки
накладывают теплый навымник. Озокерит
из первой кюветки, остывший до температуры
50—650
С, накладывают на поясницу и крестец.
Для лучшего сохранения тепла клеенку
накрывают ватником.
Лечение
тиосульфатной грелкой основано
на использовании эффекта теплоемкости
кристаллического тиосульфата натрия
при его расплавлении и последующей
активной теплоотдачи при обратной
кристаллизации. Грелка массой
500—700 г
представляет собой двухслойную
полиэтиленовую пленку, между слоями
которой в герметических камерах
содержится
2,5— 3 г
препарата.
Тепловая
ультрафиолетовая и ультразвуковая
терапия.
Лампой соллюкс и инфраруж вымя облучают
два раза в день в течении
30—60 мин.
Ее устанавливают на расстоянии
60— 80 см от
вымени.
Ультрафиолетовое
облучение проводят стационарной
ртутно-кварцевой лампой с горелкой
ПРК-2 или настольной ртутно-кварцевой
лампой с горелкой ПРК-4. Расстояние от
лампы до вымени
60—100 см,
облучение проводят в нарастающих дозах
от
5 до
20 мин.
Для ионофореза
используют портативный аппарат для
гальванизации. Электродами служат
свинцовые пластинки толщиной
2—3 мм
площадью
200—300 см2.
Вымя обмывают, высушивают полотенцем.
Густой волосяной покров выстригают,
смазывают раствором йода и покрывают
коллодием. К коже пораженной части
вымени прикладывают байковую прокладку
толщиной около
1 см,
смоченную в растворе лекарственного
вещества, с противоположной стороны—
прокладку,
смоченную физиологическим раствором.
Электроды протирают спиртом и накладывают
на обе прокладки, сверху кладут матерчатую
сухую прокладку и фиксируют их резиновыми
бинтами. Допустимая сила постоянного
тока
0,5 А на 1
см2
площади электрода. Ионофорез назначают
1—2 раза в
день по
30—60 мин.
Лечебными препаратами могут быть
1— 2%-ный
раствор новокаина, 3%-ный раствор калия
йодистого, антибиотики. Калий йодистый
и пенициллин вводят с отрицательного,
а новокаин со стрептомицином
— с
положительного электрода.
Маститы лечат
также ультразвуком. С этой целью применяют
ветеринарный ультразвуковой терапевтический
аппарат. На коже пораженной четверти
выбривают волосы, протирают ее 70°-ным
спиртом, раствором фурацилина
(1 : 5000) или
другим дезинфицирующим средством и
смазывают
50%-ным
раствором глицерина.
https://www.youtube.com/watch{q}v=JmntC55b8X4
Ультразвуковую
головку медленно передвигают по
поверхности кожи больной четверти
вымени. Процедуру начинают с малых доз
излучения—0,6—0,9
Вт/см2,
а затем увеличивают до
1,2—2 Вт/см2.
Время воздействия 5—15
мин. Ультразвуковые процедуры проводят
ежедневно. Коровы, больные серозным или
катаральным маститом, выздоравливают
через
4—6
ультразвуковых процедур.



